业务背景
- 医械研发场景核心痛点:
- 大量历史产品版本和数据信息的积累导致规划难以对齐
- 上下游信息不同步导致冗余的项目等待
- 研发经验和知识难以复用,无法快速分析总结
- 流程易变形一线执行不规范导致评审反复
- 跨部门协作黑盒导致多项目进展难管控
- 行业人才标准和研发成本高,难以及时调整资源,易造成浪费和延期等
- 细分市场规模:全球医学装备行业市场规模持续扩大,2024 年全球医学装备市场规模达到 6575 亿美元,近五年年均复合增长率达 9.54%,预测 2025 年全球医学装备市场规模将达到 6999 亿美元,其中我国体外诊断行业起步较晚,但发展较快,预测 2025 年中国体外诊断行业市场规模将达到 1399 亿元。
- 技术路径:飞书项目+飞书Aily+飞书云文档+飞书知识库+飞书会议
- 预期价值:
- 能够在医疗器械研发的专精领域拓展飞书项目的产品解决方案,拓宽市场范围,通过已有客户实践辐射更多客户的信任
- 提高飞书协同一体的方案优势,在医疗行业研发投入和人效是企业关注的重点方向之一,通过系统方案提高产品的竞争力,点亮更多企业
- 帮助客户实现IPD落地,实现流程变革,比如协作效率提升20%人效、信息获取效率提升80%、处理时效缩短至原来的10%等。
模板亮点
亮点一:端到端流程平台化管理
需求管理
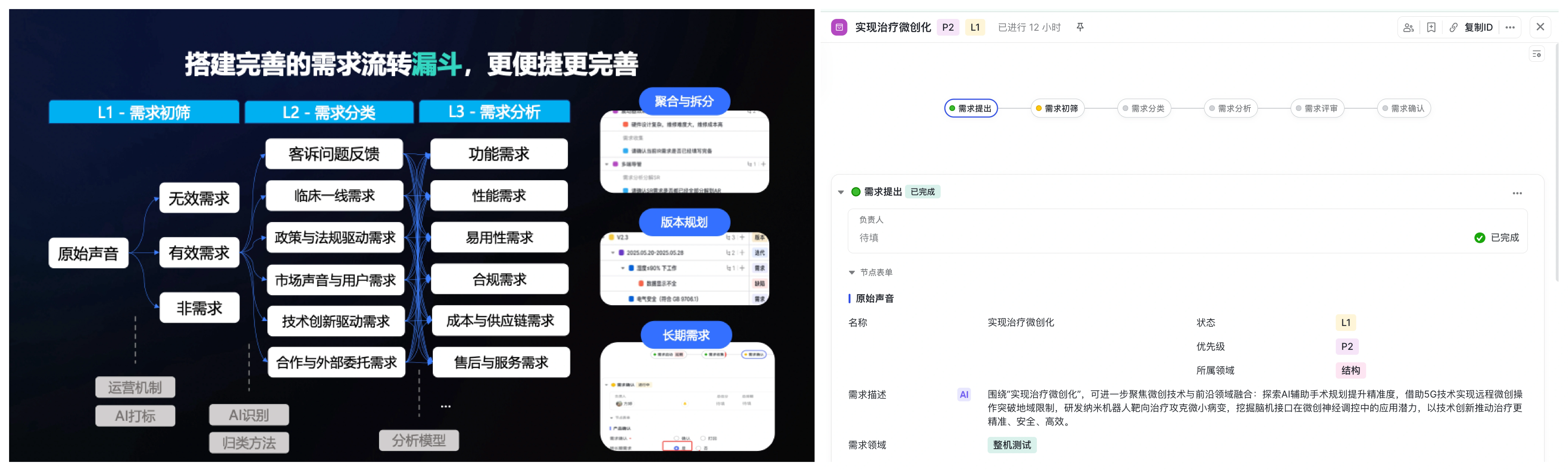
研发管理
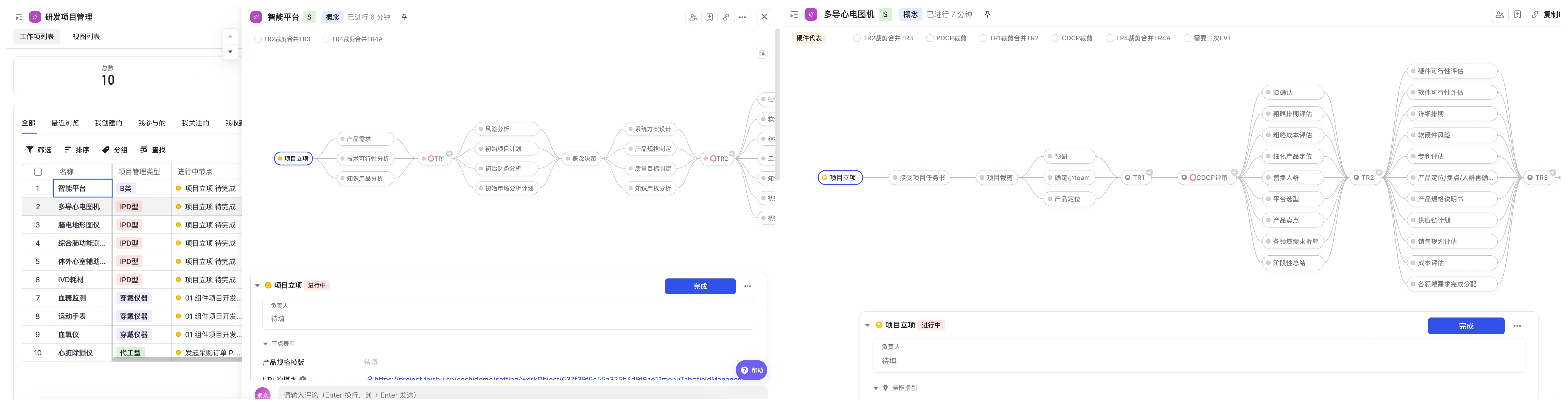
注册管理
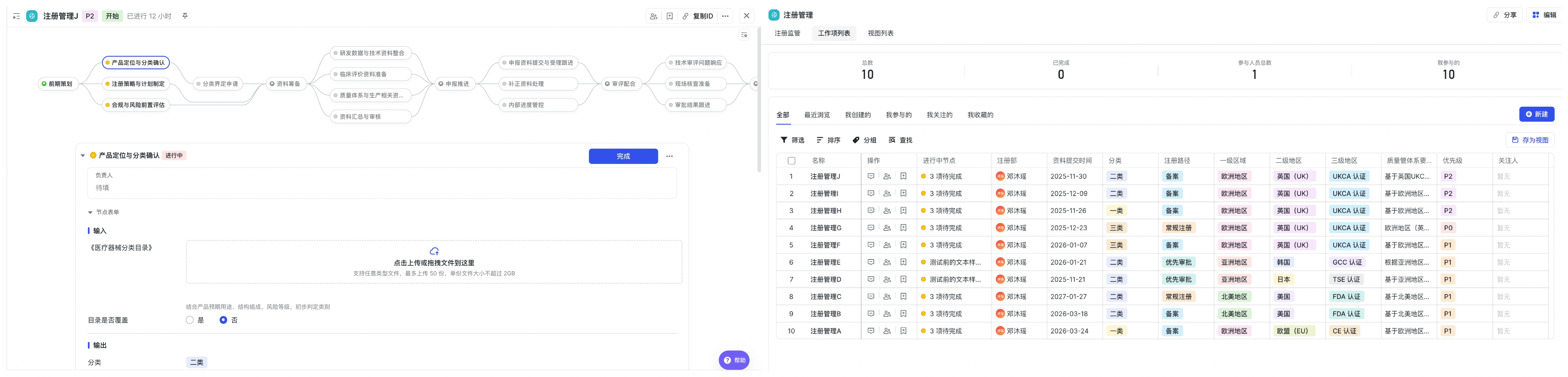
风险管理
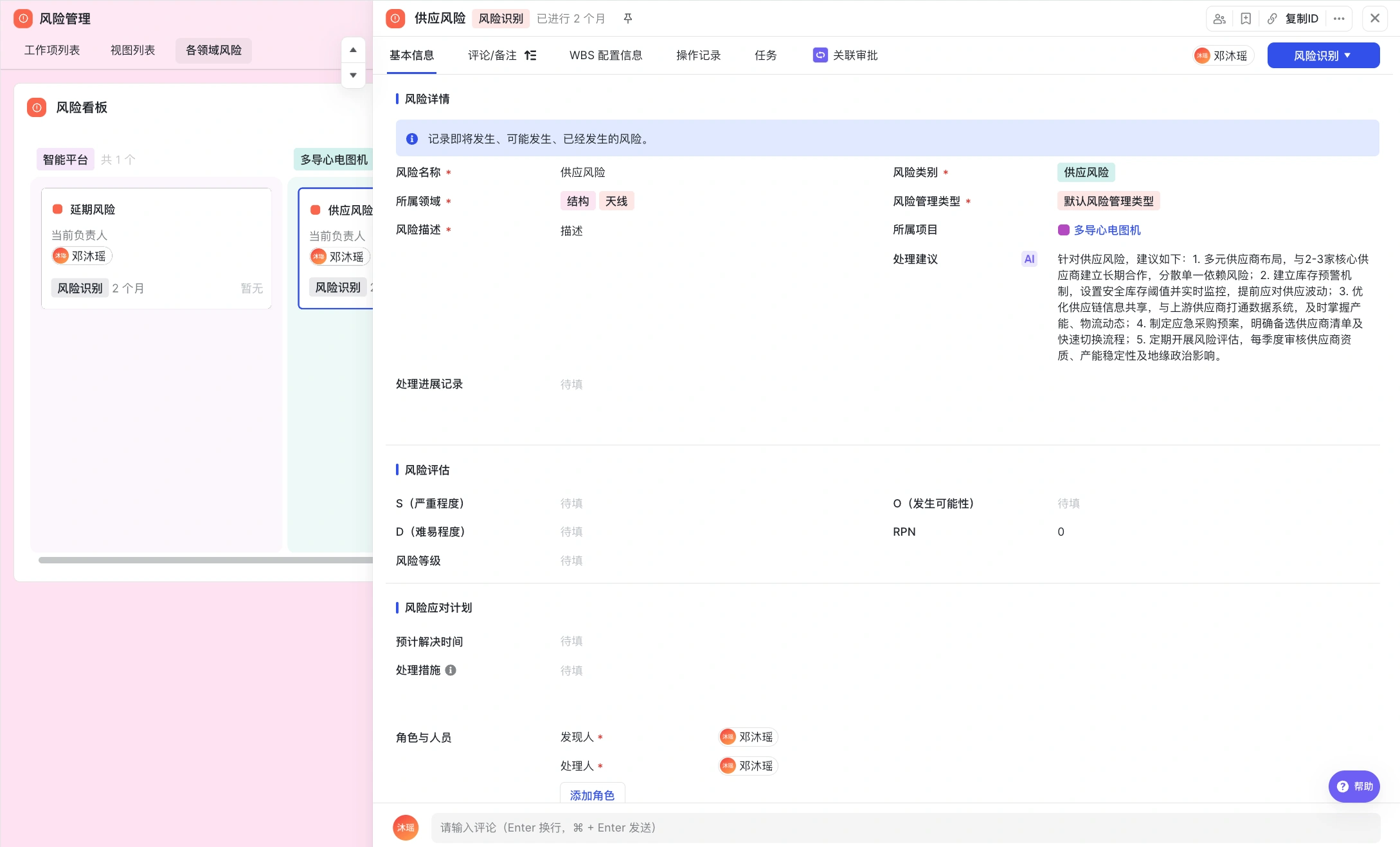
亮点二:动态看板监控
项目集穿透

风险看板
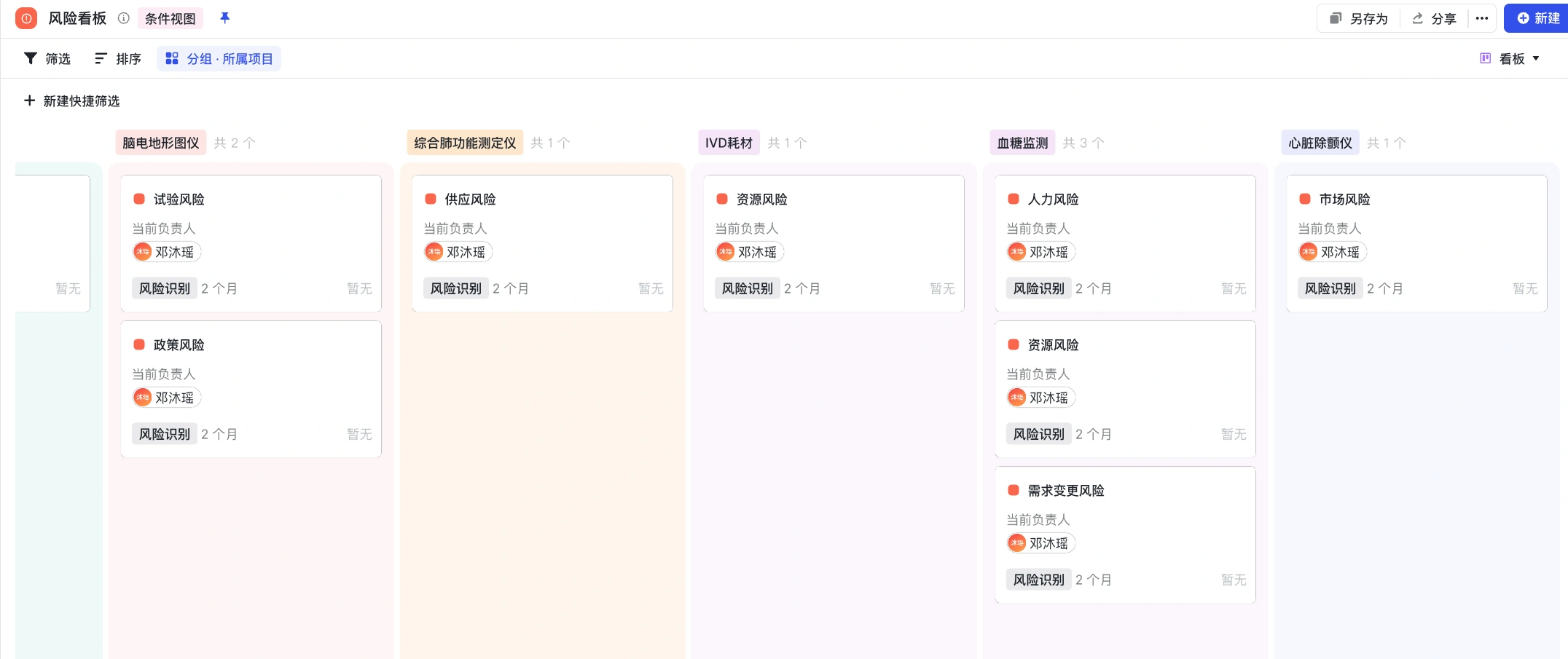
注册监管
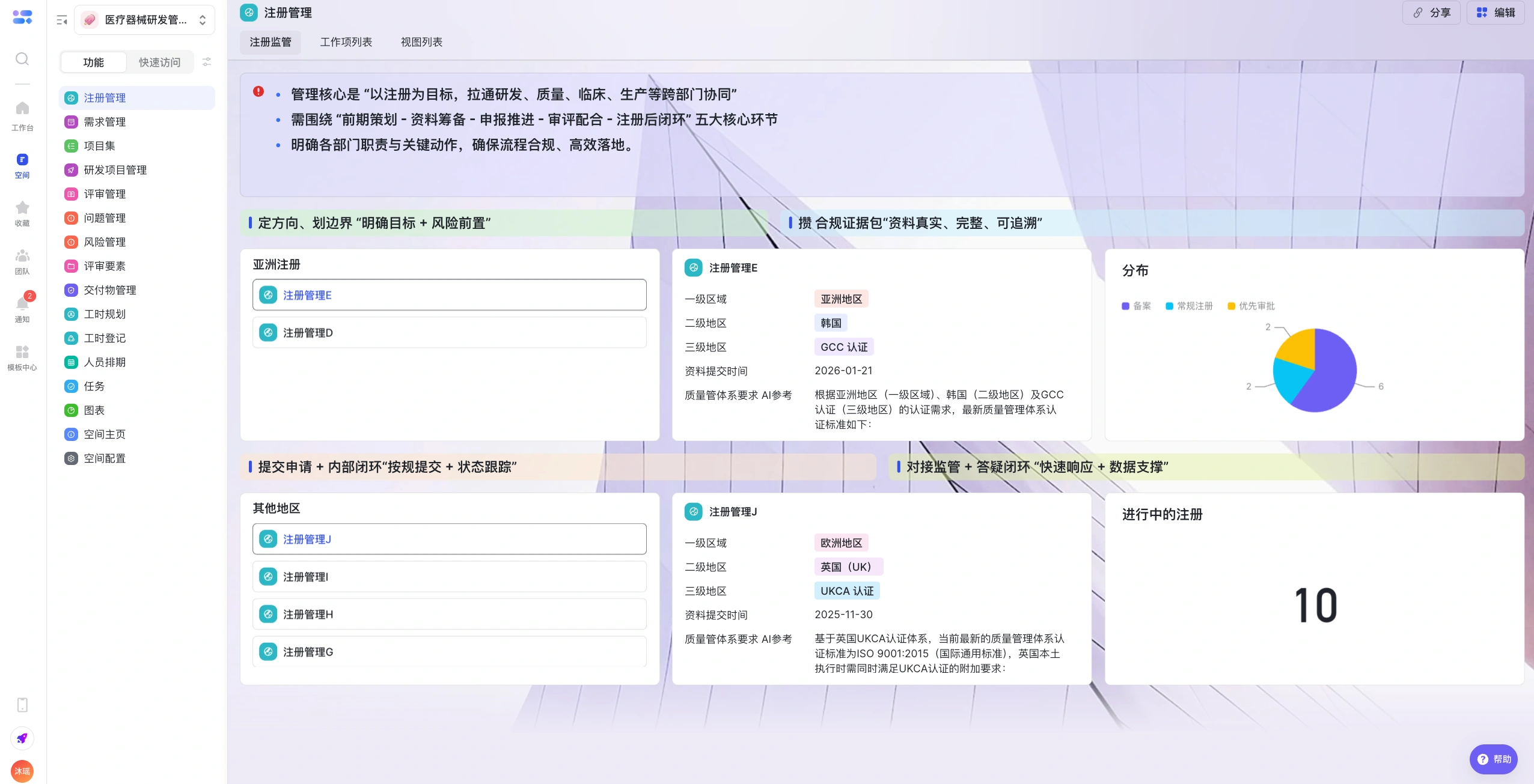
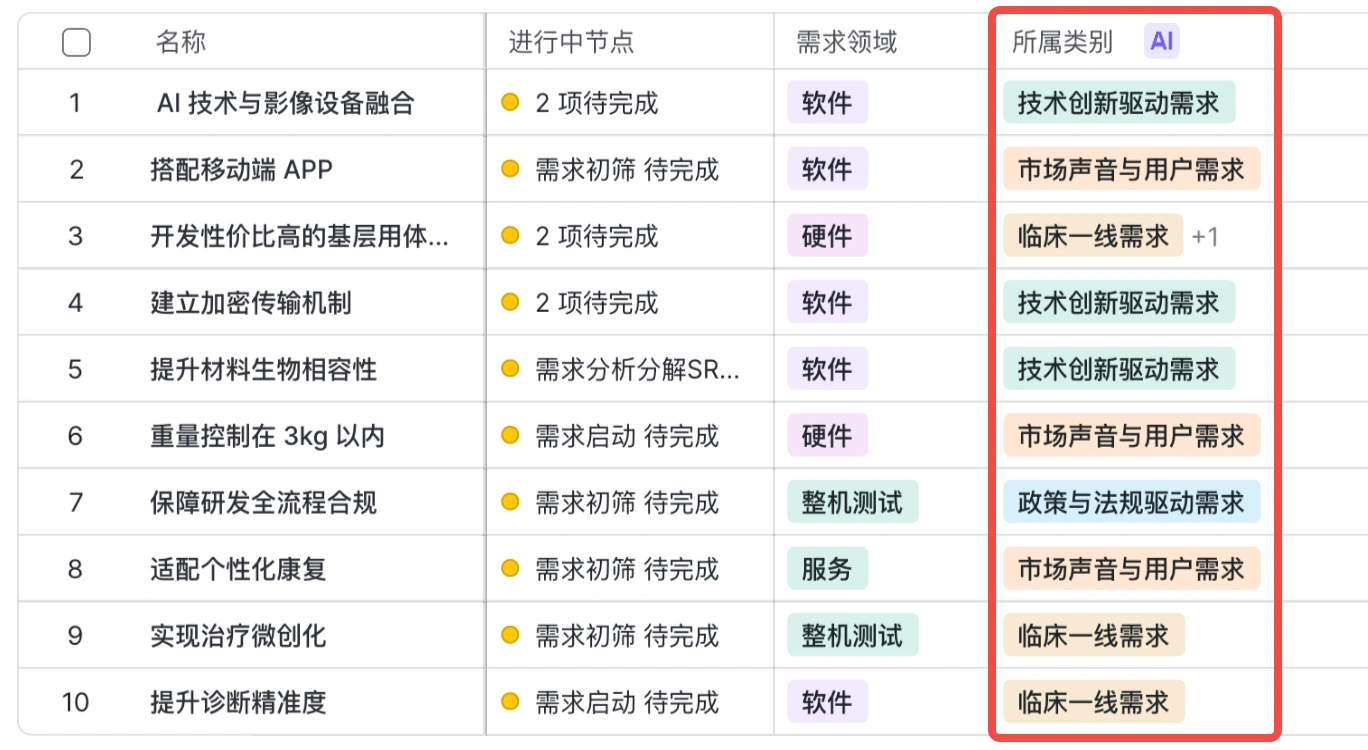
亮点三:AI赋能
需求识别并拓展
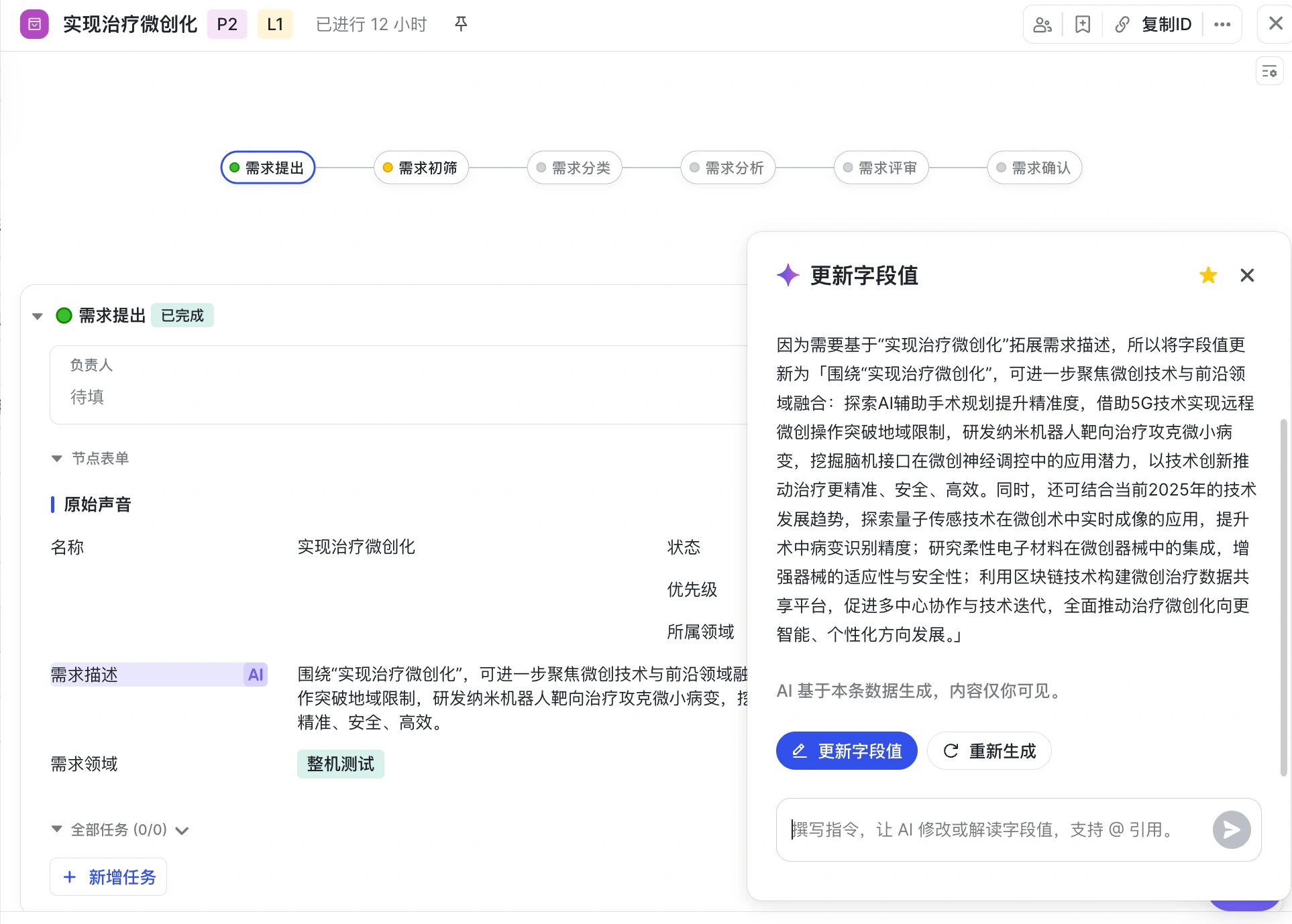
需求自动分类
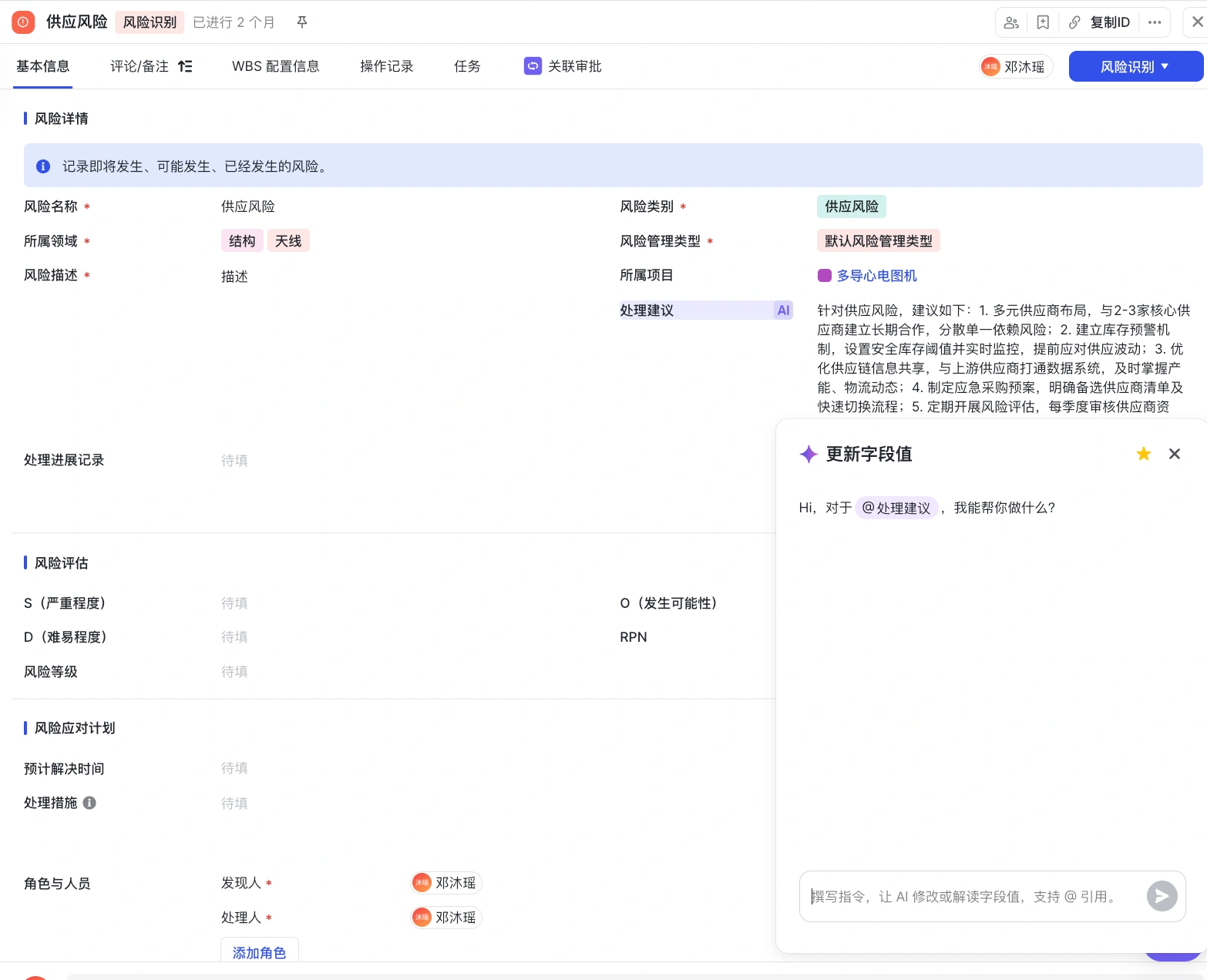
风险建议
使用介绍
整体说明
模板中设置了 项目集、需求管理、注册管理、研发项目管理、问题管理、风险管理、工时规划、评审管理 七个核心工作项,进行医疗器械研发的全生命周期管理,涵盖项目集规划、需求收集和分析拆解、注册监管、人力成本规划、质量问题监管等多个场景,开箱即用。在此基础上,支持企业根据实际业务流程进行调整,以达到最佳效果。
操作手册
当有新的需求或者客户声音需要进行管理:
- 第一步:进入需求管理,新建一个新的需求,选择“标准需求”,状态选择“L1”级别,初步选择“优先级”和“需求领域”

- 第二步:AI 自动基于需求的名称进行扩展,猜测需求的详细情况和目标,进行更细致的描述
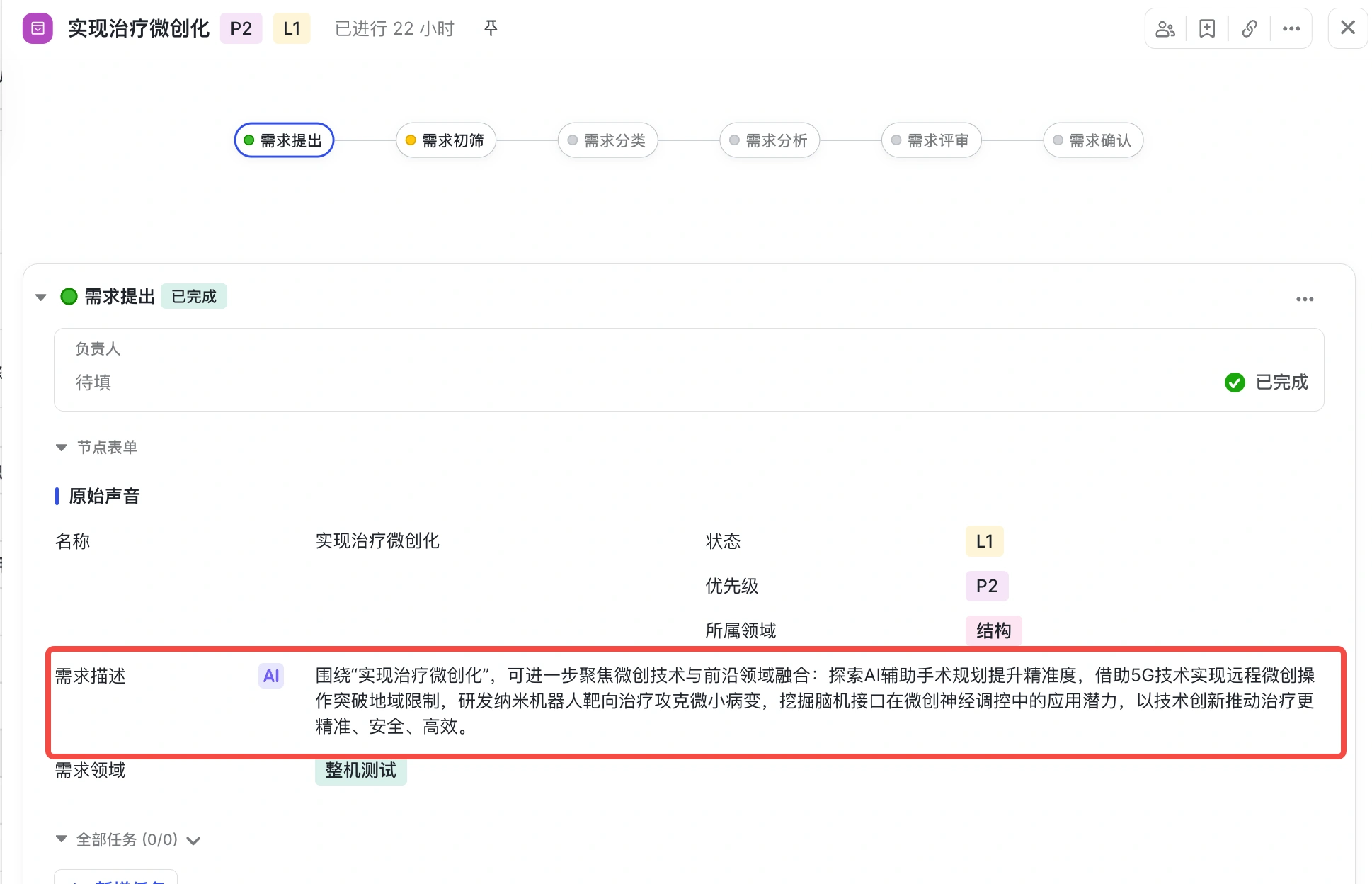
- 第三步:对需求进行初步判断,是否有效
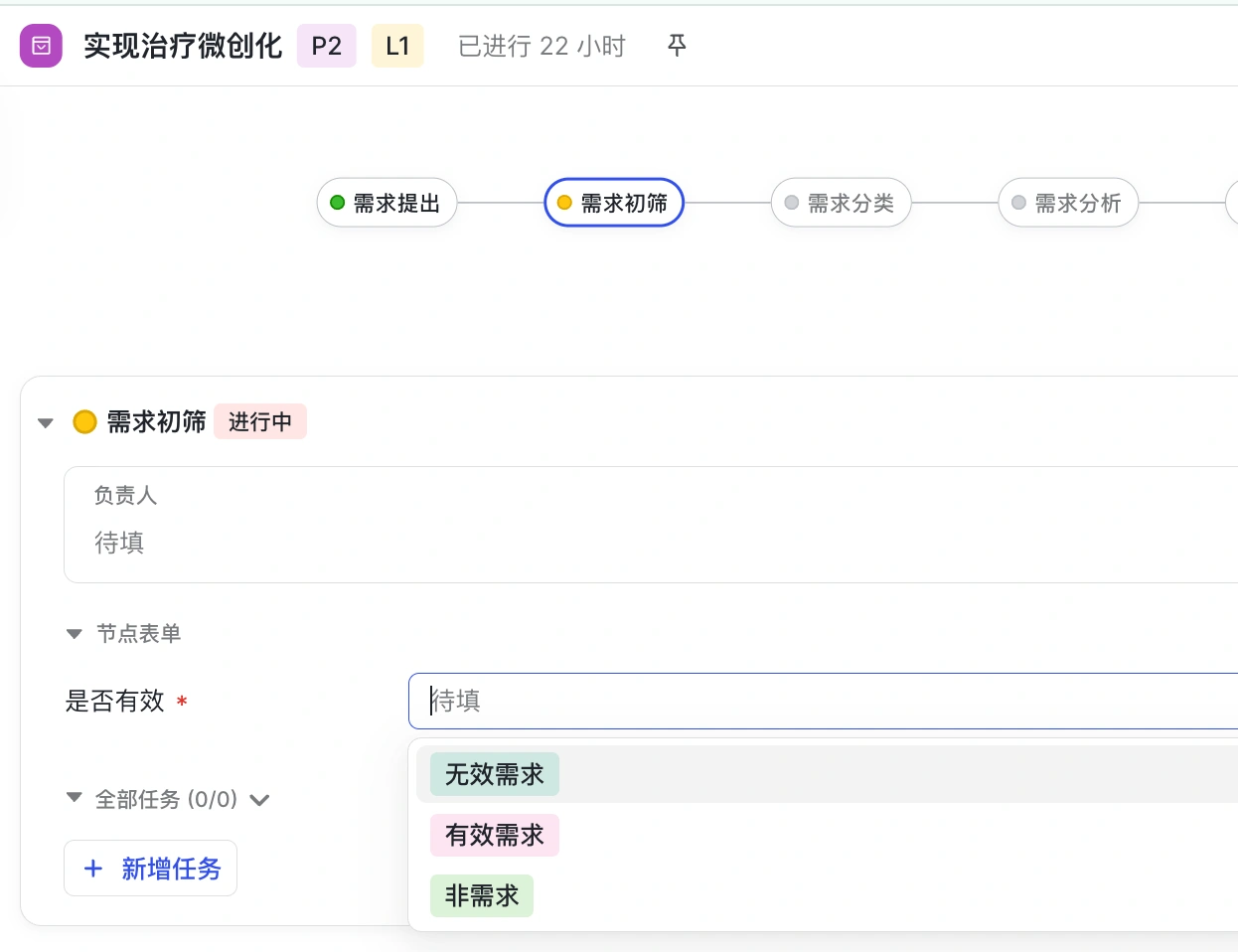
- 第四步:需求进入L2状态,由AI进行初步判断所属的类别
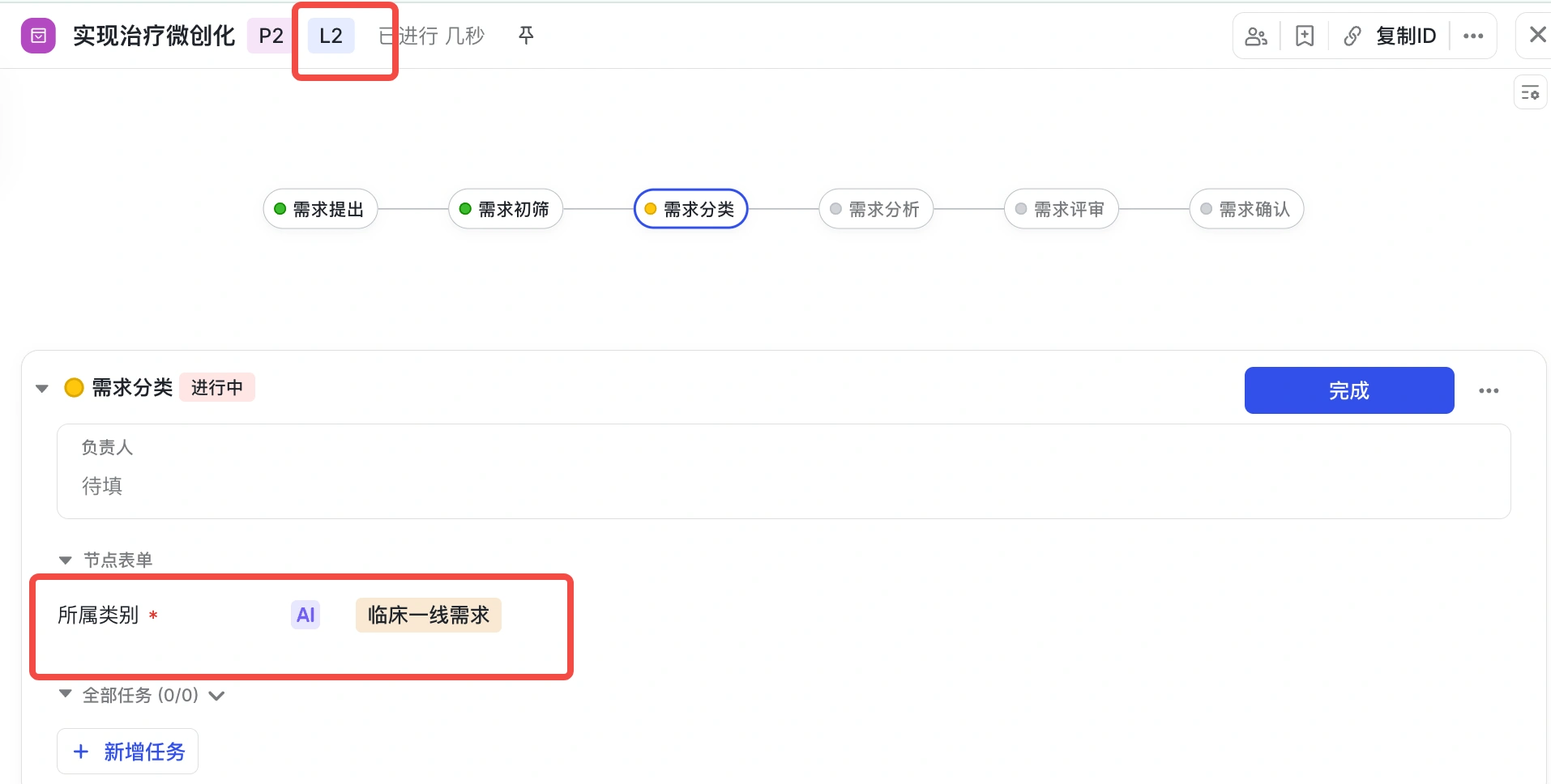
- 第五步:基于初步的类别,进一步判断内部的属性,进而完成需求评审,进入需求分发
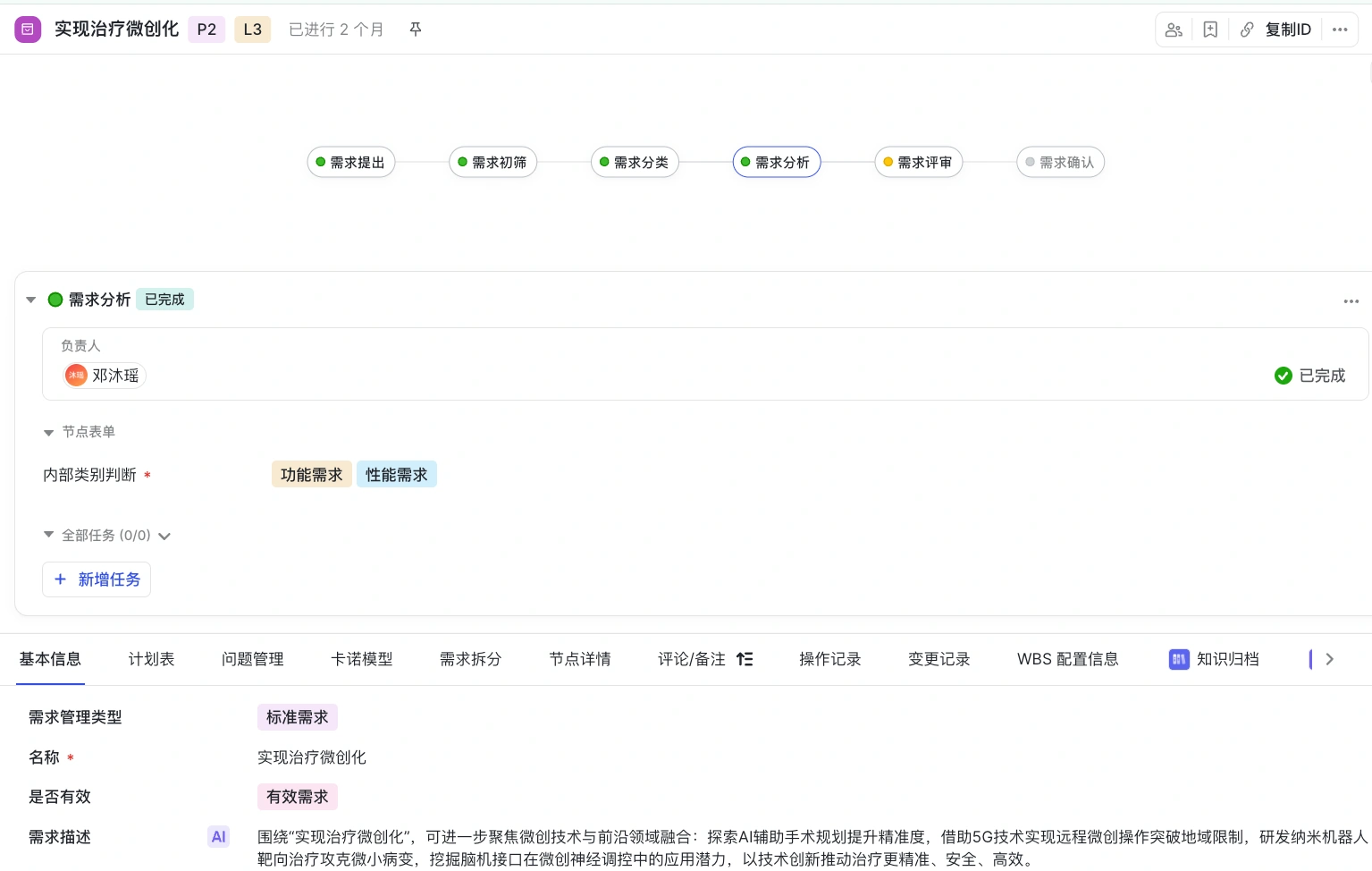
当我是项目经理或者部门经理,需要管理全貌:
- 通过“项目层层拆解视图”查看每个项目下的需求进度、相关风险。
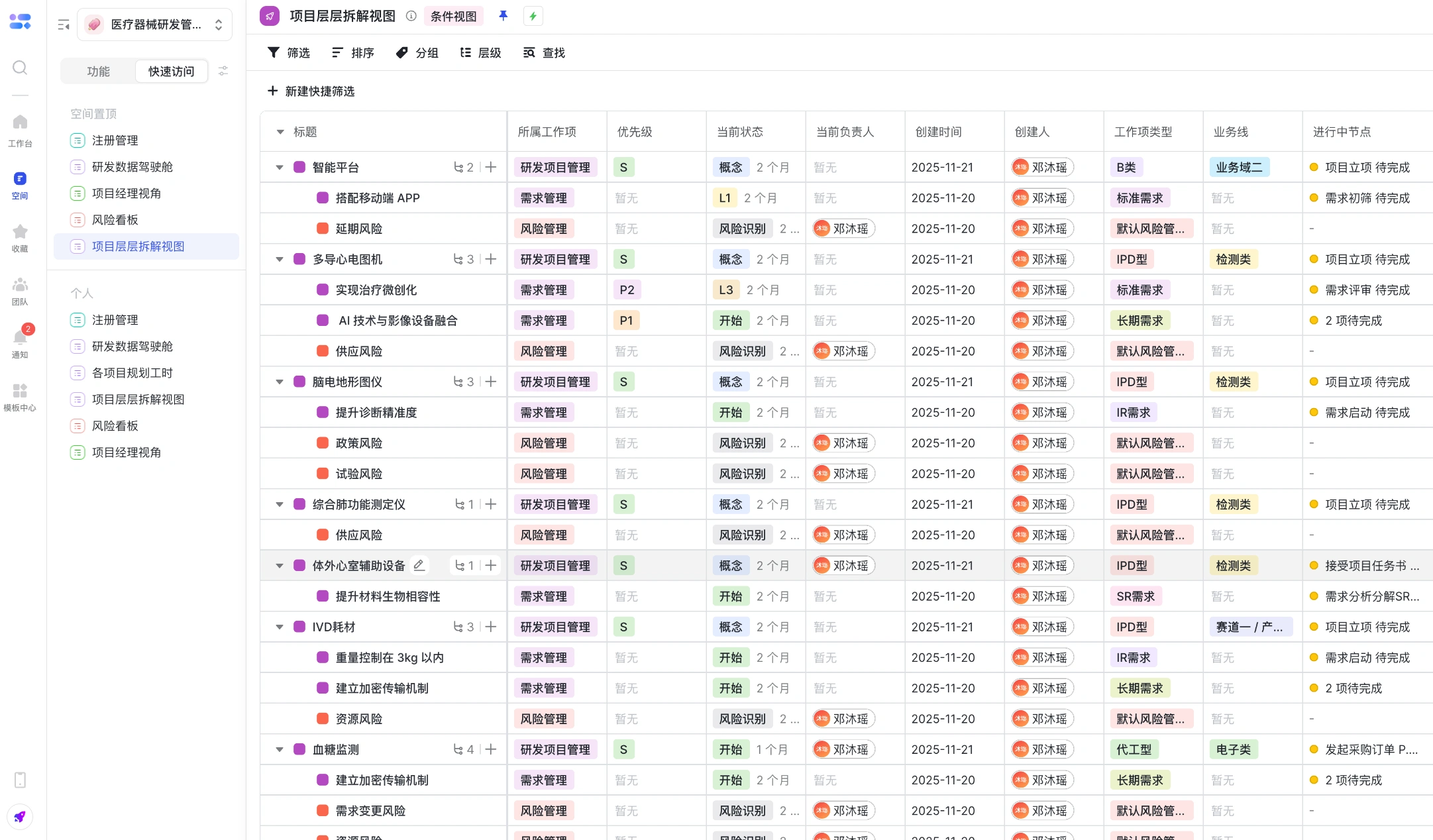
- 通过“项目经理视角”查看公司每个项目集下的项目表现和风险、成本、进度指标表现。

- 通过“风险看板”掌握每个项目下的风险表现和处理进展。

当我需要对产品注册进行管理:
- 进入“注册管理”新建,选择类别、一级地区、二级地区、三级地区等信息
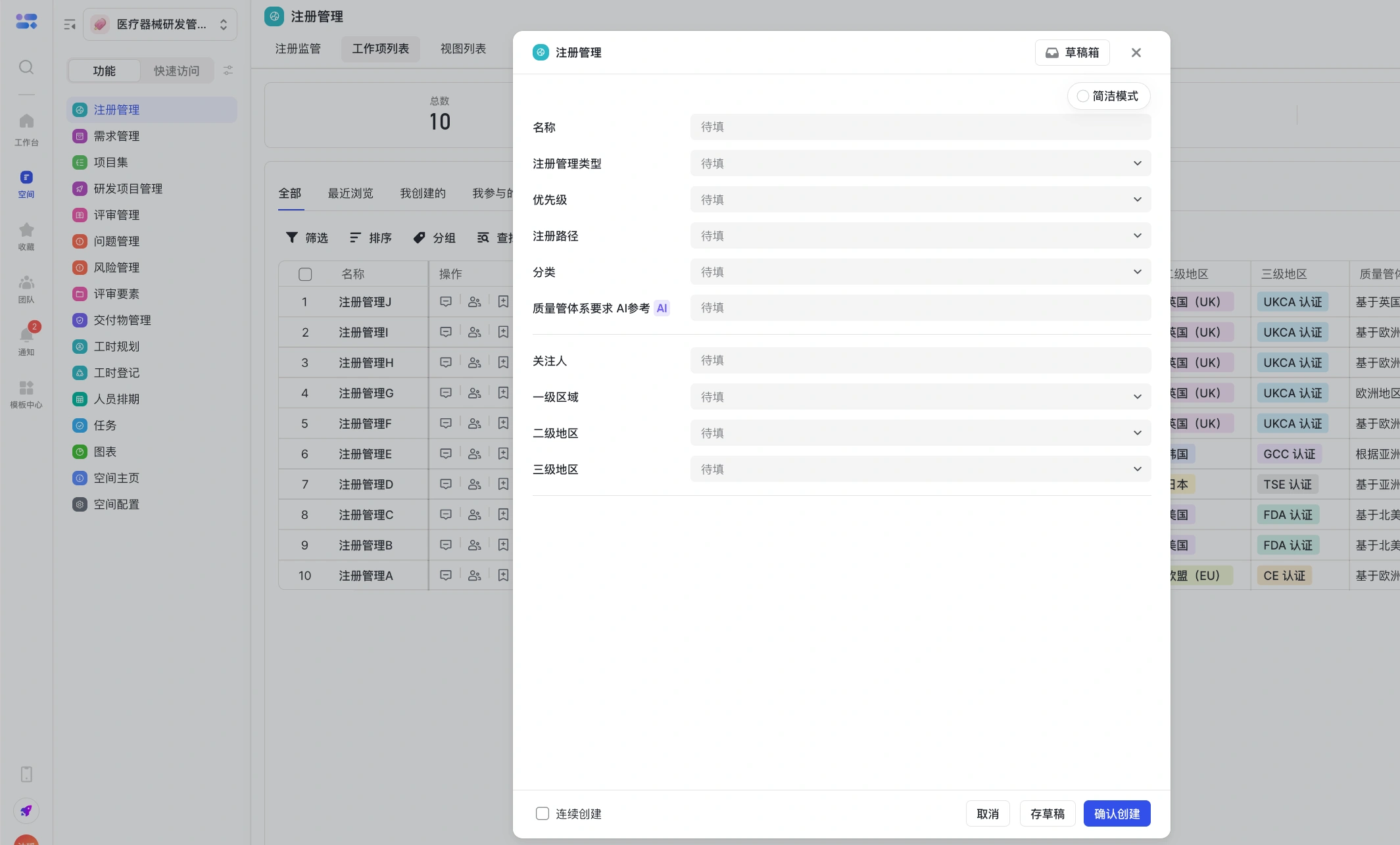
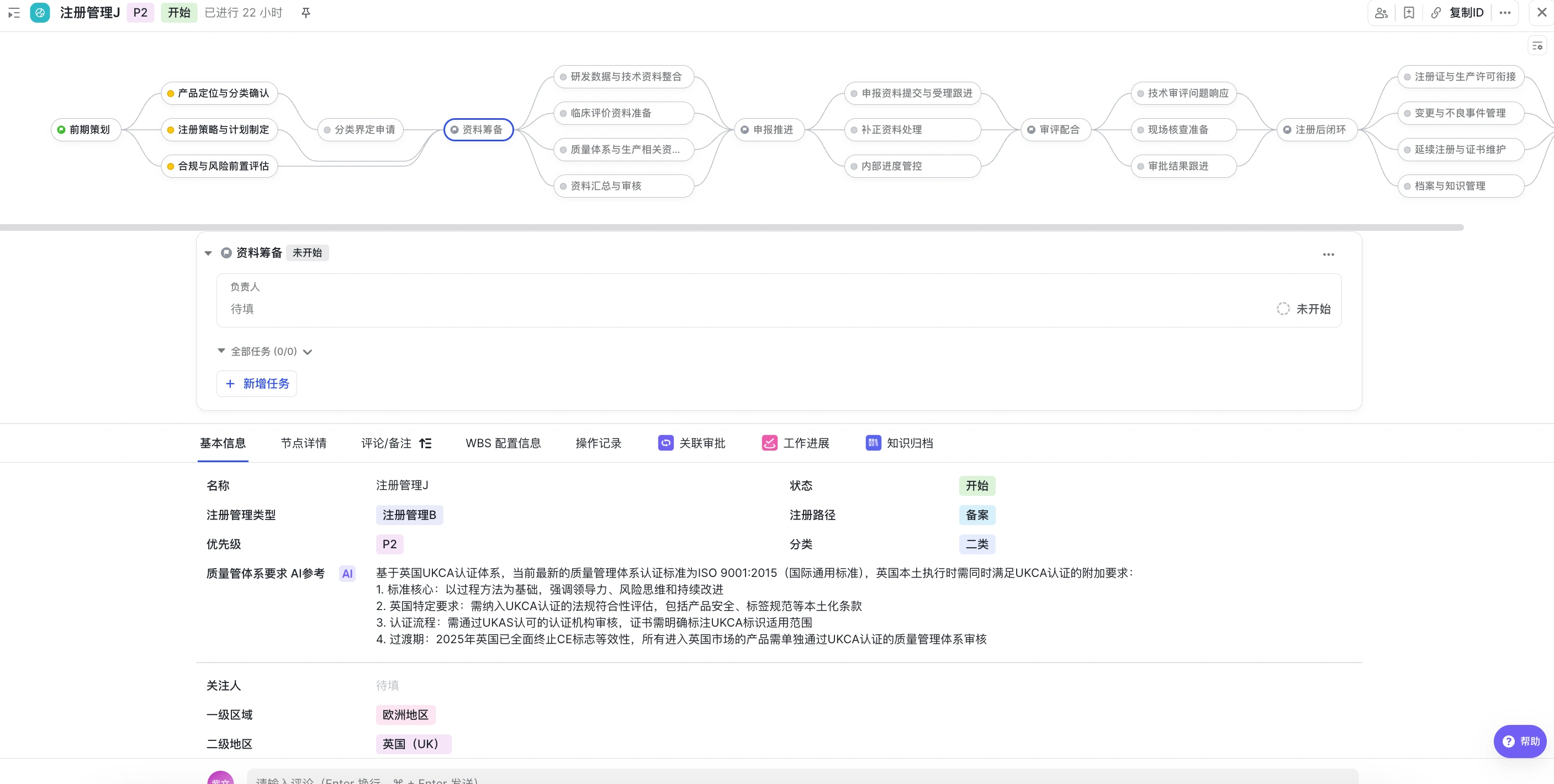
- 进入内部管理的起点 - 注册前期策划,需避免 “研发与注册脱节”,核心由注册部牵头,联合研发、质量、市场、临床等部门完成。
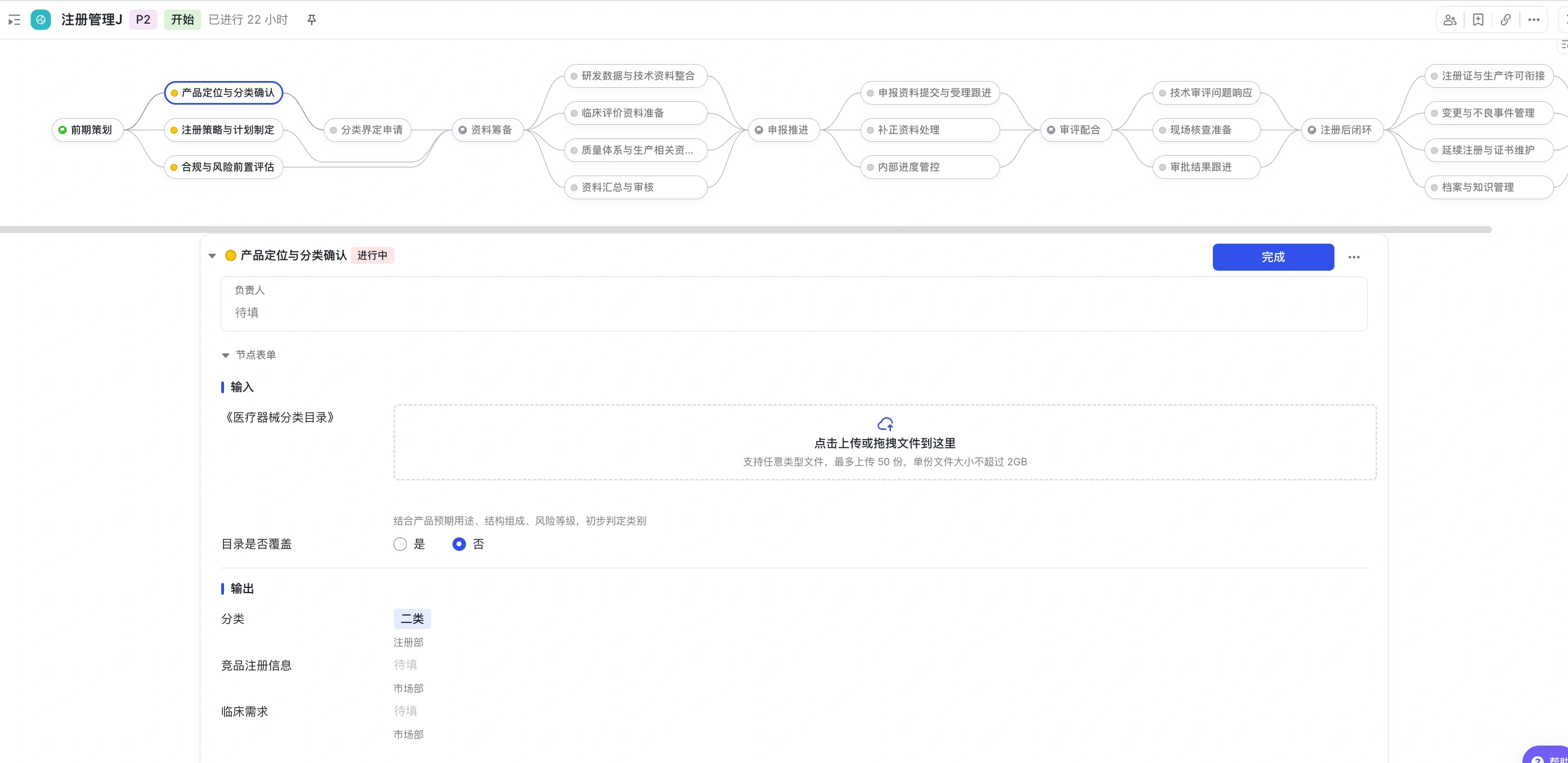
- 进入内部管理的核心环节 - 注册资料筹备,需确保所有资料符合 NMPA《医疗器械注册申报资料要求》,由注册部统筹,研发、质量、生产、临床等部门分工提供核心资料,避免 “资料缺漏、数据矛盾”。以此类推
- 过程中设置了节点裁剪,比如注册部对照《医疗器械分类目录》,结合产品预期用途、结构组成、风险等级,初步判定类别,若目录未覆盖,启动 “分类界定申请”(准备产品说明、技术原理等资料,对接省级药监局或 CMDE),形成《产品分类确认报告》,避免后续因分类错误返工。